Спайк-белок коронавируса сам по себе вызвал нарушения свертываемости крови
Биологи провели микроскопические исследования образцов крови здоровых людей с добавленным спайковым белком коронавируса и без него, а также пациентов, больных ковидом. Исследователи заметили, что добавление в кровь свободного S-белка вызывало формирование амилоидных сгустков и изменения формы клеток крови. Кроме того, ученые смоделировали ток плазмы в сосудах и экспериментально показали, что у пациентов с ковидом он может быть сильно затруднен. Препринт статьи опубликован на портале medRxiv.
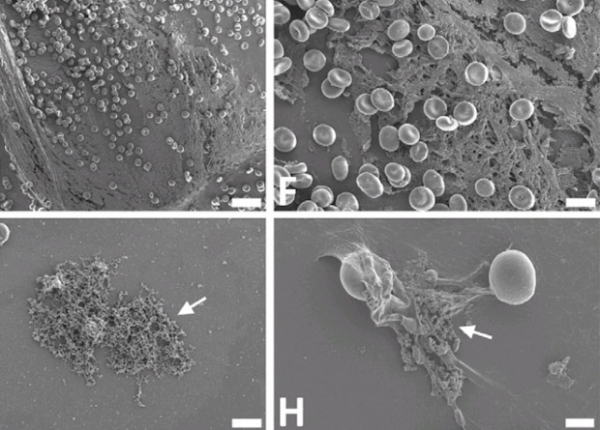
Lize M. Grobbelaar et al. / medRxiv, 2021
Вызываемую SARS-Cov-2 инфекцию можно охарактеризовать беспрецедентными для других респираторных инфекций патологиями. Среди них – нарушения свертываемости крови (коагулопатии), которые могут приводить либо к кровотечениям, либо тромбозам. Связывание спайкового S-белка с рецепторами в момент проникновения вируса в клетку может вызывать клеточные патологии, но само по себе не может объяснить такую распространенность коагулопатии у пациентов. Однако S-белок путешествует в организме и сам по себе отдельно от вируса, высвобождаясь из инфицированных клеток: его, например, находили в мочеиспускательном канале. Частицы этого белка также могут проникать сквозь гематоэнцефалический барьер.
Ученые из Университета Стелленбоша под руководством Итерезии Преториус (Etheresia Pretorius) изучили способность частиц S-белка взаимодействовать напрямую с тромбоцитами и белком фибриногеном, вызывая в нем изменения и, как следствие, нарушения свертываемости крови. Сначала исследователи при помощи флуоресцентной микроскопии проверили, накапливаются ли аномальные амилоидные комплексы в плазме здоровых людей с добавлением частиц S-белка и без них. В образцы с добавлением одного нанограмма на миллилитр S-белка добавляли тромбин (активатор коагуляции) и делали микрофотографии. В тех образцах, куда попал вирусный белок, формировались более плотные фибриновые сгустки. В образцах цельной крови спайковый белок вируса вызывал гиперактивацию тромбоцитов.
Плазма здоровых людей без добавления спайк-белка (А) и с ним (В). После добавления тромбина в образцах с S-белком
формируются более плотные сгустки.
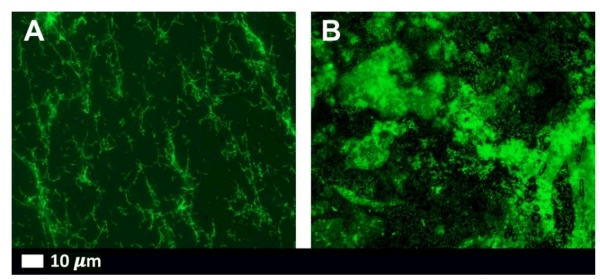
Lize M. Grobbelaar et al. / medRxiv, 2021
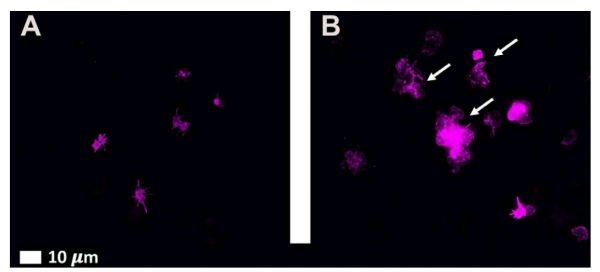
После добавления спайкового белка эритроциты начинали склеиваться, у тромбоцитов разрасталась мембрана.
Lize M. Grobbelaar et al. / medRxiv, 2021
После добавления спайкового белка эритроциты начинали склеиваться, у тромбоцитов разрасталась мембрана.
Lize M. Grobbelaar et al. / medRxiv, 2021
Напоследок, исследователи проверили, как S-белок влияет на ток плазмы в проточных камерах шириной 400 микрометров и высотой 100 микрометров. Камеры обработали тромбином, а затем в течение пяти минут со скоростью 10 микролитров в минуту вводили образцы плазмы здоровых людей, смешанные со спайк-белком образцы, а также образцы пациентов с коронавирусной инфекцией. За время эксперимента в образцах плазмы здоровых людей постепенно сформировались лишь небольшие сгустки на дне камеры. В плазме с добавленным спайк-белком сформировались волокнистые и бесформенные сгустки. Быстрее всего среагировала на тромбин плазма пациентов: примерно за 90 секунд бесформенные сгустки заняли основной объем камеры, препятствуя току жидкости.
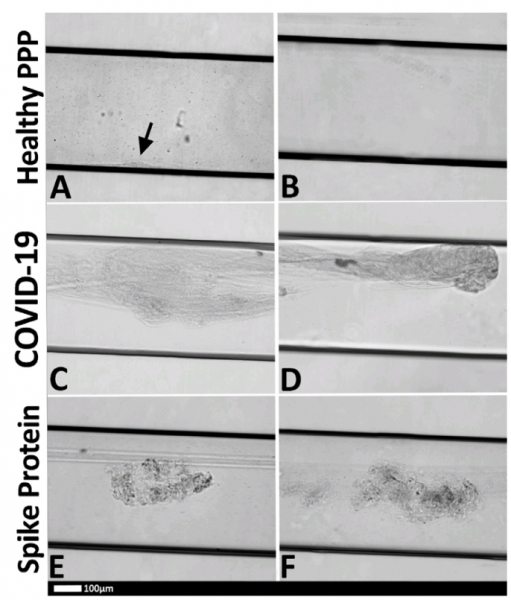
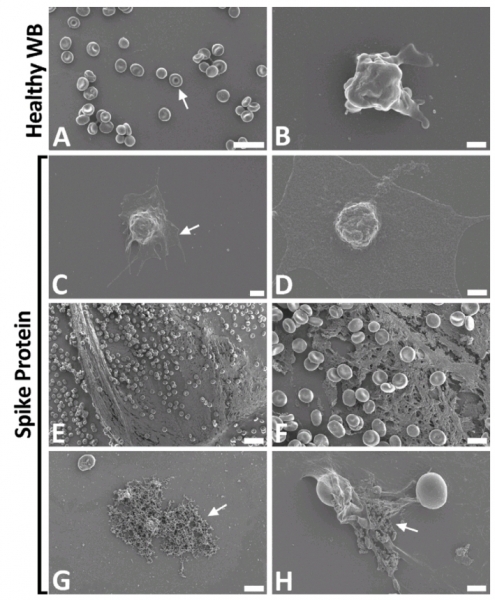
Камеры с плазмой здоровых людей (А, В); пациентов с COVID-19 (C, D); здоровых людей, в образцы добавили спайк-белок (E, F).
Lize M. Grobbelaar et al. / medRxiv, 2021
Авторы работы предполагают, что, нацеливая вакцины и потенциальные лекарственные средства против S-белка, есть вероятность облегчить течение заболевания и снизить риск тромботических осложнений.
Проблема возникновения тромбозов у пациентов с коронавирусной инфекцией, а также здоровых людей, получивших вакцину от коронавируса, волнует многих специалистов. Ранее ученые выяснили, что риск развития нарушения свертываемости крови и осложнений после COVID-19 примерно в восемь раз выше по сравнению с вакцинацией.

